전기방식에 필요한 전반적인 검사 방법 장비 사용법등을 시리즈로 함께 공유하고자 합니다. 또한 내용 중 배관에 대한 전기방식 내용이 많은 점 이해 바랍니다. 제가 배관유지관리만 해봐서... 많은 부분은 IPS에서 참조했습니다.
전기방식에 발전을 위해서 많은 의견 주시고 부족한 건 함께 발전시켜 나가길 바랍니다.
기준 전극
기본적인 내용을 잘 설명해 줘서 참고했습니다.

•전극 전위차
- 전지를 구성하는 두 전극의 종류가 다르기 때문에 두 전극(금속) 사이의 전위(potential)의 차이(difference)가 발생.
- 전압(voltage) : 두 전극 간의 전위(potential) 차이
예) Fe -450mV [SEC] Mg -1,600mV [SEC] 전압은 1,150mV
•기준 전극 (reference electrode)
- 전극 전위의 절댓값 측정은 불가능. 측정되는 전압은 항상 두 전극 사이의 전위 차이일 뿐.
- 전극의 절대적인 potential energy를 측정하기 힘들기 때문에 기준전극을 정해놓고 그에 따라 상대적인 potential energy를 측정함. 만약 reference 전극이 바뀌면 전압값이 달라질 것.
- 기준전극으로의 저항을 매우 높게(모든 전위차계(테스터포함)의 입력 임피던스는 10MΩ이상, 매우 중요)하여 기준전극으로는 전류가 흐르지 않게 함. 그러면 인가한 전압이 그대로 작업전극에 걸림.
- 기준 전극을 기준으로 전극 A, B에 대한 각각 전위의 상대적인 값이 측정됨.
- 만약 전극 A의 전위가 기준 전극 R의 전위보다 1.0V 높고 전극 B의 전위가 0.5V 낮을 경우, 전극 A와 전극 B의 전위 차이는
1.0 - (-0.5) = 1.5V가 됨.
•표준 수소 전극 (standard hydrogen electrode, SHE)
- 전위의 기준이 되며 표준으로 많이 사용.
- 산 용액에 잠긴 백금(Pt) 전극 표면에 수소 기체를 불어넣으면, 수소 기체와 산 용액에 있는 수소 이온은 산화 환원 평형에 도달함.
H2⇌2H+ + 2e- (Pt)
- 괄호 속에 Pt를 표기한 것은 백금은 산화 환원 반응에 참여하는 것이 아니며, 단순히 전자의 전달체로서 역할.
- 위 반응이 표준 상태 조건(수소 기체의 압력은 1 bar, 동시에 수소 이온의 활동도 역시 1인 조건)에서 평형에 도달했을 경우를 기준으로 삼고, 그것을 표준 수소 전극이라 함.
Pt | H2 (1bar) | H+ (aq. a=1)
- 표준 수소 전극의 전위를 모든 온도에서 0V로 정함.
•노말 수소 전극 (normal hydrogen electrode, NHE)
- 수소 기체압력이 1 bar이고, 동시에 용액에서 수소 이온의 활동도가 1인 조건을 만들기가 쉽지 않음.
- 따라서 농도가 1M인 염산 용액을 사용한 수소 전극을 기준전극으로 사용한 것이 노말 수소 전극.
- 수소 이온의 활동도가 정확히 1은 아니지만 표준 수소 전극의 전위와 비교하여 전위 차이가 매우 작고, 실험실에서 쉽게 반복해서 제작할 수 있음.
- 수소 전극과 Ag/AgCl을 짝지어 만든 전지
[출처] 1. 전기화학 셀, 전극 전위|작성자 Winho
좀 어렵긴 한데 설명을 잘해주셨네요 Winho님 감사합니다. https://blog.naver.com/bshte1440/222507952165
🐰 반쪽 전지 半쪽電池 (Half-Cell) :
산화 반응과 환원 반응이 일어나는 각 부분(+,-)의 전지. 전지는 산화 반응과 환원 반응이 일어나는 부분을 염다리나 격막 등으로 분리시켜 놓아 전자가 도선을 통해 이동하도록 만든 장치이다. 강관과 기준전극은 전위차가 발생함으로 전지가 되어 각각 + 혹은 - 극성을 가지는 전지의 반쪽이 된다. 그러므로 기준전극은 전지의 한쪽, 극성에 관계없이 전지의 반쪽을 말한다. 그래서 반쪽전지라 한다. 보통 기준전극을 "0"전위[기준]로 하고 이 값의 상대적인 값 [전위차]을 전위하고 합니다.
수소전극은 실험실용으로 사용하고 있어 생략하고 현장에서 사용하는 전극을 위주로 설명하겠습니다.
일반적으로 전위 측정에 사용되는 전극은 다음과 같습니다.
‑ 구리/황산구리 전극
‑ 은/염화은 전극
‑ 아연 전극
이들 전극의 전위에 대한 대략적인 비교는 그림 1에 나와 있습니다.
Cu/CuSO4 전극은 매설 구조물의 방식 수준을 측정하는 데 사용되는 가장 일반적인 유형의 전극입니다. Ag/AgCl 은 부두, 해양 플랫폼, 선박 선체 및 기타 해양 구조물과 같은 수중 구조물의 잠재적인 측정에 널리 사용됩니다.

순수 아연 전극은 해양 구조물 및 저장 탱크 바닥 아래에서 영구 기준 전극으로 사용할 수 있습니다.
전위 측정의 신뢰성은 소나 전위 장치와 같은 정교한 시스템을 사용하여 향상될 수 있습니다.
A.1 기준 전극
전기화학적 시리즈에서 주어진 금속의 전위는 전위가 ±0mV로 임의로 설정되는 소위 "표준 수소 전극" SHE와 관련됩니다. 이러한 전극은 수소 이온 활성도가 1인 용액에 담근 백금 와이어 또는 백금 메쉬로 구성되며 대기압(760 Torr = 1.013 ×105 Pa)에서 수소 가스로 플러시 됩니다.
이러한 전극을 취급하는 것은 당연히 매우 어색합니다. 따라서 실제로는 소위 기준 전극으로 대체됩니다. 가장 중요한 기준 전극과 SHE에 대한 전위는 그림 A.1에 나와 있습니다. 이들의 특성은 표 A.1에 나와 있습니다.
A.1.1 구리/황산구리 전극
A.1.1.1 매설 파이프라인 및 기타 매설 구조물의 보호 전위 수준을 측정하는 데 사용되는 가장 일반적인 유형의 전극은 구리/황산구리 기준 전극입니다.
일반적인 구리/황산구리 전극은 그림 A.2에 나와 있습니다.


메모: 위 표에서 0.1N과 1.0N은 각각 0.1과 1.0 "정상 용액"을 의미합니다.
A.1.1.2 황산동 전극은 전극이 깨끗하게 유지된다면 광범위한 토양 조건에서 사용되고 있습니다. 테스트 키트에는 황산동 전극이 2 개 이상 있어야 합니다. 동일한 토양에 나란히 설치했을 때 둘 사이의 전위차를 측정하여 일치 여부를 주기적으로 확인하여야 합니다. 최상의 성능을 위해서는 전위차가 약 10mV를 초과해서는 안 됩니다. 차이가 너무 크면 둘 중 하나가 오염된 것입니다. 이 경우에는 세척하고 새로운 용액으로 다시 채워야 합니다. 구리 막대는 10% 질산 용액에 몇 분 동안 담가서 청소할 수 있습니다. 다시 조립하기 전에 증류수로 잘 헹구어야 합니다. 전극은 용액이 포화 상태를 유지하도록 몇 가지 과잉 황산구리 결정 또는 분말과 함께 포화 황산구리 용액으로 가득 차 있어야 합니다. 오염을 방지하기 위해 용액은 정기적으로 새로운 용액으로 교체되어야 합니다. 다공성 플러그는 건조를 방지하기 위해 사용하지 않을 때 덮어두어야 합니다. 전극이 마르면 다공성 플러그를 교체하십시오.





메모: 다공성 물질로 만들어진 플러그를 통해서 땅과 접촉한다.
A.1.2 은/염화은 전극
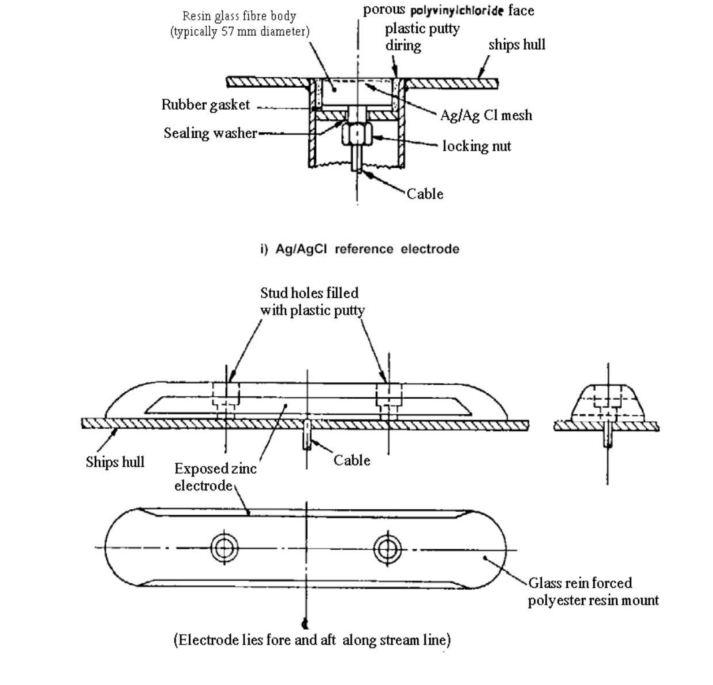
이 전극은 음극 방식으로 보호되는 해저 파이프라인, 방파제, 부두, 플랫폼 및 물탱크 내부의 전위 측정에 널리 사용됩니다. 황산동은 염화물 이온에 의해 오염될 수 있으므로 해수에서의 사용이 제한됩니다. 그림 A.3은 전형적인 은/염화은 반쪽(Half-Cell) 전지를 보여줍니다.

A.1.3 순수 아연 전극
아연은 바닷물에서 전위가 불안정하기 때문에 정확한 전극으로 간주되어서는 안 됩니다. 이는 방식 수준을 추정하는 데에만 사용됩니다.
아연 전극은 수명이 길기 때문에 영구 전극으로 사용할 수 있습니다. 이 전극은 저장탱크 바닥 중앙 등 접근이 어려운 곳에 사용할 수 있습니다. 아연에 대한 판독값은 아연의 종류와 표면 상태에 따라 달라집니다. 해수와 토양 모두에서 변동은 50mV 범위에 있습니다. 그림 A.4는 다양한 유형의 아연 전극을 보여줍니다.

메모: 백필이 충진 된 내부에 아연이 있다. 수명이 길어 영구기준전극으로 사용했으나 포화황산동과 전위값이 달라 지금은 현장에서 많이 사용하지 않고 있다.


A.1.4 칼로멜 전극
칼로멜 전극은 포화 염화칼륨 또는 일반 염화칼륨 용액과 접촉하는 수은‑염화수은 혼합물로 만들어진 반쪽 전지입니다(표 A.1 참조). 용액은 구리/황화구리 전극과 동일한 방식으로 다공성 플러그를 통해 전해질과 접촉합니다. 칼로멜 전극의 안정적인 반전지 전위는 교정 목적에 적합합니다. 실험실 유형의 전극은 일반적으로 유리로 구성됩니다.
이상으로 기준전극에 대해 알아 자세히 알아봤습니다. 엿날 자료긴 해도 기본적인 내용은 현재와 같습니다.
다양한 기준전극이 있으므로 각 상황에 따라 선택해서 사용하면 됩니다. 육지에 배관에는 포화황산동 기준전극이 가장 많이 사용되고 있습니다.
'전기방식 > 검사 및 장비 활용' 카테고리의 다른 글
| PCM+ (Pipeline Current Mapping System) (0) | 2024.05.27 |
|---|---|
| 지하매설물 탐측 (0) | 2024.02.21 |
| 접지저항 측정 (0) | 2022.08.31 |


